松田 諭
( Discovery of novel anti tumor substances from the marine actinobacteria and chemical investigations of salinisporamycin )
海の生態系を構成している生物の一部は、その環境に適応するために、 陸棲生物とは異なる天然物を生産していると思われる。 海洋性天然物の生産者は、おもに、細菌や微細藻類等であり、これら微生物の生産物のなかには、 生物の活性を抑制・阻害する物質、すなわち、医薬品・農薬になる可能性、または半合成品の原料も含んでいると考えられる。 つまり、海洋性微生物は、多くの有用な生理活性物質を生産している可能性がある。 そのため、海洋性微生物の探索は有効であり、これら微生物を採取するためには、食物網、共生、生態系の適応性、 系統分類等の幅広い視点から捉えて行なう必要がある。 そして、これらの試行錯誤によって発見された海洋性微生物は、その付随する結果として、 有用な生理活性物質を生産しているかもしれない。 本研究では、海洋性微生物のうち、抗生物質の生産能が高いと考えられている放線菌に注目し、 とりわけ、南半球の環太平洋地域にある沿岸で採取された海洋性放線菌の生産する抗癌物質を探索した。
海洋性放線菌に由来する抗癌物質を効率よく選抜していくために、新規抗癌物質探索システムであるLC-MS screening法を構築した。 LC-MS screening法とは、抗癌物質の最適な発酵生産条件、ヒト肺癌由来細胞を用いた抗癌活性試験 (A549活性)、 粗抽出物の画分化とHPLC/PDA-ESI/MS (LC-MS)等を用いた化合物の簡易同定を一括して行なうことができる選抜方法である。 LC-MS screening 法の利点は、海洋性放線菌の培養から既知物質の同定まで2~3 週間程度の短期間で終了することと、 微量物質の同定が可能なことであった。 そのため、LC-MS screening法は、海洋性放線菌の生産する抗癌物質を迅速、かつ簡便に同定できると思われた。
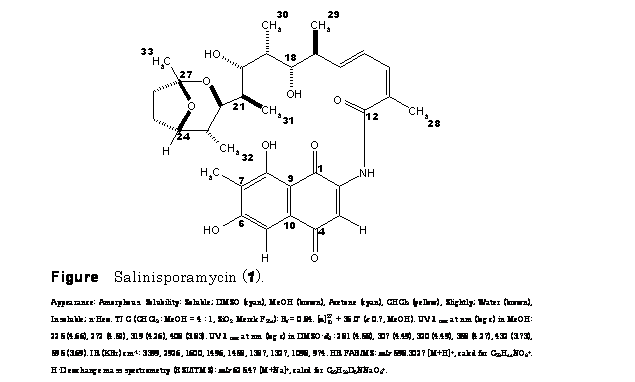
続けて、LC-MS screening法で除外できなかった新規rifamycin 類抗癌物質の salinisporamycin (1 ) 1)について述べる (Figure)。 1 生産株は、ミクロネシア連邦ヤップ州N: 9°31'11.0"、E: 138°10'26.7"のsedimentsより採集され、 Salinispora arenicola CNH-643に極めて近い菌株 (YM23-082)として同定された2)。 1 の単離・精製は、YM23-082由来A549活性物質群のLC-MSスペクトルを指標にして行なった。 1 は、2箇所の部分構造で構成されており、その一つであるansa 鎖部分構造は、 S. arenicola に由来するsaliniketal類と同様であり、もう一方のnaphthoquinone部分構造は、天然物として初めての発見であった。 そのため、1 は、種特異的なrifamycin生合成経路の代謝物であることが示唆された。 1 の生理活性は、A549活性と抗菌活性であり、とりわけ、A549活性は、 rifamycin 類の抗癌活性に関する新しい知見であった。 特徴的な現象として、1 は、各溶液中で色調変化していた。
1 の発酵生産、単離・精製について述べる。 1 を大量発酵生産する前に、1 生産株と思われる17菌株の生理活性を比較し、 もっともA549活性と抗菌活性の強いYM23-082を選定した。 YM23-082の大量培養には、海水とPharmamediacを含む培養液を用いた。 発酵生産後、1 の単離・精製は、おもに吸着カラムクロマトグラフィー (シリカゲル)と 分取用HPLC/PDA 3)で行なった。 以上の単離操作により、10L分のYM23-082培養物あたり0.6 mgの1 を得た。
1 の構造決定、互変異性、生理活性について述べる。 1 の構造決定は、おもにNMRによる解析であり、とりわけ、bi-cyclic構造は、 C-27位の13C NMR ケミカルシフト(DMSO-d6; C 104.2, CD3OD; C 106.6)、ならびに、 それに相当するketal基のIRスペクトル ( C―O 1098 cm-1)、そして、ROESYプロットの相関ピーク (H-22/H-25a, H-22/H-26a) によって決定した。 1 のソルバトクロミズムは、naphthoquinone母核内のC-1位-C-8位間とC-6位-C-8位間によるketo-enol互変異性だけでなく、 amide-imide互変異性によって共役系も拡張していることが考えられた。 1 の生理活性は、A549細胞に対してIC50 = 3 g/mlの抗癌活性、 ならびに Staphylococcus aureus IFO 12732、Bacillus subtilis IFO 3134に対して、 それぞれ、MIC = 0.5μg/ml、MIC = 4.1μg/mlの抗菌活性が認められた。
--------------------------
1. Matsuda S, Adachi K, Matsuo Y, Nukina M, Shizuri Y (2009) Salinisporamycin, a novel metabolite from Salinispora arenicola. The Journal of Antibiotics, 62 (9): 519-526.
2. YM23-082の16S rRNA塩基配列(1395-bp)は、BLAST上で S. arenicola CNH-643と100 %の相同性を示した。
3. 分取用HPLC/PDAにInertsil ODS-2: 4.6 mm i.d. x 250 mm (GL-science Inc.)を接続した。